Лекция 2

Лекция 2
1. Лекция 2. Классификация катализаторов
Лекция 2. Классификация катализаторов
Гетерогенный катализ осуществляется в том случае, когда катализатор и реагирующая система находятся в различных фазовых состояниях. Для объяснения многих примеров гетерогенного катализа привлекаются представления теории промежуточных соединений. Например, при каталитическом разложении пероксида водорода происходит расходование, а затем регенерация катализатора, оксида марганца (IV).
Все гетерогенные процессы происходят на поверхности фазового раздела. Больше всего изучены те гетерогенные процессы, при которых молекулы газовой фазы реагируют с поверхностью твердого тела. Гетерогенный катализ на твердой поверхности может быть объяснен на основе представлений теории адсорбции.
Адсорбционная теория гетерогенного катализа
Термин адсорбция означает накопление молекул на поверхности раздела фаз. (Необходимо различать термины адсорбция и абсорбция. Последний означает проникновение молекул в объем другого вещества.) Различают адсорбцию двух типов. Физическая
Гетерогенный катализ обычно включает как физическую адсорбцию, так и хемосорбцию. Некоторые химики полагают, что механизм гетерогенного катализа включает пять названных ниже стадий, причем все они обратимы.
1. Диффузия. Реагирующие молекулы диффундируют к поверхности твердог вещества.
2. Адсорбция. Реагирующие молекулы сначала подвергаются физической адсор( ции на активных центрах поверхности твердого вещества. Затем они хемосорбируютс на ней.
3. Химическая реакция. Реагирующие молекулы, оказывающиеся рядом друг другом, вступают в реакцию между собой с образованием продуктов.
4. Десорбция. Эта стадия обратна стадии адсорбции. После завершения реакции молекулы продуктов оказываются сначала хемосорбированными на поверхности. Затем они становятся физически адсорбированными на ней и в конце концов высвобождаются с поверхности.
5. Диффузия. Молекулы продуктов диффундируют от поверхности.
Эти пять стадий схематично представлены на рис. 9.20 на примере каталитического гидрирования этилена с использованием тонкоизмельченного никелевого катализатора:
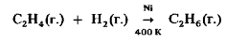
Отметим, что водород адсорбируется на поверхностных атомах никеля в атомарном виде. Тонкоизмельченное состояние катализатора обеспечивает большую площадь его поверхности и тем самым повышает эффективность его каталитического действия.

Роль носителей в катализаторах.
1) До середины XX в.: носитель – инертный материал, ответственный за поддержание дисперсного состояния активного компонента
2) Конец XX в.: “носитель может и должен рассматриваться как активная часть каталитической системы, так как между носителем и активным компонентом может происходить достаточно сложное взаимодействие вплоть до образования химических соединений” (Э.Б.Стайлз, Носители и нанесенные катализаторы. Теория и практика. М.:Химия, 1991)
Требования к носителям
► Носитель должен быть индифферентен в отношении основной каталитической реакции и не ускорять побочных процессов, которые могут привести к снижению селективности
► В случае бифункциональных катализаторов носитель должен обладать определенными кислотными (или другими) свойствами
► Носитель должен быть инертен к активному компоненту или же не должен образовывать с ним неактивных соединений
► Требование инертности не отрицает возможности или даже необходимости проявления носителем промотирующих и модифицирующих функций þ
Изучение процессов взаимодействия активного компонента с носителем, приводящих к образованию как активных, так и неактивных соединений – одна из важных проблем научных основ приготовления нанесенных катализаторов
► Носитель должен обладать высокой термической стабильностью в условиях каталитического процесса
► Носитель должен быть химически инертен к компонентам реакционной среды и в условиях регенерации катализатора
► Носитель должен обладать оптимальной величиной удельной поверхности
► Носитель должен обладать оптимальной пористой структурой
► Носитель должен обладать необходимыми механическими свойствами, теплопроводностью, а в ряде случаев – электропроводностью, которые предопределяются условиями эксплуатации катализатора
► Носитель должен обладать определенной нанотекстурой поверхности и набором поверхностных функциональных групп как для требуемого взаимодействия с предшественниками активного компонента на стадиях приготовления, так и для фиксации частиц активного компонента в конечном катализаторе
Развитая поверхность носителя гарантирует существенное увеличение эффективности превращения реагентов в различных химических процессах.
Носитель для катализатора насыпного типа, обладающий развитой поверхностью, характеризуется многочисленными внутренними отверстиями и рациональной геометрической формой носителя. Развитая поверхность носителей гранулированного типа обеспечивается благодаря малому размеру гранул и открытой пористой структуре.
В промышленности применяют катализаторы:
- в виде цилиндров, гранул диаметром несколько миллиметров,
- катализаторы, получаемые нанесением активного агента (платины, палладия) на пористый носитель - активированный уголь, кизельгур, силикагель, алюмогель.
Количество каталитически активного металла в нанесенном катализаторе не превышает нескольких процентов, что дает возможность экономить драгоценные дефицитные металлы.
Из-за очень малых концентраций нанесенного металла на поверхности носителей находятся не микрокристаллы, а небольшие группы атомов, которые Кобозев назвал ансамблями. Он обратил внимание на то, что за увеличением количества нанесенного металла на носителе активность нанесенного катализатора проходит через максимум.
Для повышения активности, термодинамической устойчивости, механической жесткости применяют катализаторы в виде многокомпонентных систем - смешанные и промотированные. Смешанные катализаторы - это смесь двух или нескольких оксидов Al2О3, Сr2О3, СаО и МgO, активность которых является функцией состава.
Специфической особенностью гетерокаталитических процессов является способность катализатора к промотированию и отравлению.
Промоторы (активаторы), не имеют каталитические свойства, но повышают каталитическую активность катализатора. Например, для железного катализатора для синтеза аммиака нужен промотор оксид алюминия. Он покрывает тонкой пленкой поверхность катализатора и защищает его от рекристаллизации, сохраняя дефекты в поверхностном слое, т.е. удельную активность катализатора.
Отравление – резкое снижение активности катализатора в присутствии некоторых веществ (т. н. каталитических ядов). Для реакции синтеза аммиака (катализатор – губчатое Fe), присутствие в реакционной смеси соединений S вызывает резкое снижение активности железного катализатора; в то же время способность катализатора к адсорбция реагентов снижается очень незначительно.
Активные центры • Для объяснения особенностей гетерогеннокаталитических процессов Г. Тэйлором было высказано следующее предположение: каталитически активной является не вся поверхность катализатора, а лишь некоторые её участки – т.н. активные центры, которыми могут являться различные дефекты кристаллической структуры катализатора (например, выступы либо впадины на поверхности катализатора).
Активные центры – свободные участки поверхности, где могут адсорбироваться молекулы реагирующих веществ. Другая часть поверхности катализатора занята адсорбированными молекулами примесей. Число активных центров на единицу поверхности зависит от природы и способа приготовления катализатора.
Сравнение типов катализа О сходстве механизмов гетерогенного и гомогенного катализа можно судить по тому, что стадия хемосорбции в первом аналогична стадии образования промежуточного соединения во втором. Различие их состоит в том, что на поверхности гетерогенного ка тализатора, благодаря наличию нескольких типов активных центров, могут образовываться различные типы активированных комплексов, приводящих к появлению разных продуктов реакции. В результате гетерогенные катализаторы характеризуются более низкой селективностью, чем катализаторы в гомогенном катализе.
