Лекция 1

Лекция 1
1. Лекция 1. Понятие о катализе и катализаторах
Катализаторы играют исключительно важную роль в живой природе. Почти все реакции в живых организмах сами по себе происходят медленно и только благодаря участию биологических катализаторов протекают с достаточной для организмов скоростью.
Первым случаем сознательного применения
катализаторов считается образование этилового эфира из спирта с помощью серной
кислоты, открытое в VIII веке. Крупное промышленное использование катализа осуществлено в 1746
году в камерном способе производства серной кислоты.
В конце
XVIII века открыто каталитическое действие кислот при осахаривании крахмала и
впервые применены твердые катализаторы: глины при дегидратации спиртов, металлы
в процессах дегидрирования. Однако понятие о катализе возникло позднее. Лишь в
1834 году Митчерлих ввел понятие «контактные реакции», а в 1835 году Берцелиус предложил
термин «катализ».
Из распространенных ныне в промышленной практике твердых катализаторов первой была открыта и получила широкое применение металлическая платина. В первой четверти XIX века открыто ускоряющее действие платины в реакциях разложения пероксида водорода, окисления водорода, оксида углерода и углеводородов, окисления спирта в уксусную кислоту. В 1831 году Филлипс запатентовал применение платины для окисления диокисда серы. Однако резкое снижение активности платины при переработке сернистого газа, полученного обжигом колчедана, препятствовало ее промышленному применению.
Причина этого явления – отравление платины
соединениями мышьяка и другими ядами – была установлена лишь в конце XIX
столетия. Только после этого были разработаны способы очистки газов от контактных ядов и возник
крупномасштабный промышленный каталитический процесс – контактное окисление диоксида серы. Ныне открыты тысячи катализаторов, несколько
сот из них находят применение в гетерогенном и гомогенном катализе.
Самыми
крупнотоннажными катализаторами являются алюмосиликаты.
Их широко
применяют в каталитической переработке нефтепродуктов как в качестве собственно
катализаторов, так и в виде прочных пористых носителей
для
металлов и оксидов в различных процессах.
Большая часть мономеров и полученных из них полимеров являются продуктами каталитических процессов переработки углеводородов и их производных, полученных из нефти, угля, сланца, природного газа. Каталитические процессы играют важную роль в производстве моющих средств, красителей, лекарственных веществ. Основной органический синтез, дающий полупродукты и продукты органической технологии, базируется в основном на каталитических реакциях.
Катализаторами являются вещества, которые
участвуют в элементарных
физических
и химических стадиях химической реакции, изменяют скорость
химической
реакции, но после завершения химического процесса выделяются в неизменном химическом виде в реакционную
смесь. Превращения реагентов
под
действием катализаторов называется катализом.
Катализ может быть двух видов:
- положительный (ускоряет реакцию)
- отрицательный (замедляет химическую реакцию).
В присутствии катализатора возможно ускорение
в миллионы раз. Обычно катализатор многократно вступает во взаимодействие, повышая скорость
реакции в течение длительного времени и образуя продукты, масса которых
превосходит массу катализатора в тысячи раз. Для классификации удобно выделять агрегатное
состояние катализаторов и реагентов. По агрегатному состоянию катализаторы могут находиться в
газообразном, жидком и твердом состоянии. Реагирующие вещества также могут
находиться
в газообразном, жидком и твердом состоянии.
Если катализатор и реагенты находятся в одном и том же агрегатном состоянии, то такие системы называют гомогенными и катализ называют гомогенно - каталитическим.
Если катализатор и реагенты находятся в разных
агрегатных состояниях,
такие
системы называют гетерогенными и катализ – гетерогенным. Практический же
интерес составляют жидкие и газообразные системы с твердым катализатором.
К гетерогенным катализаторам относятся:
- металлические;
- оксидные;
- металоксидные;
- кислоты (кислотно-ионнообменные смолы, алюмосиликаты и др.);
- различные металлы на кислотном носителе.
Гомогенные системы:
- кислоты, основания;
- комплексы металлов;
- галогенидные комплексы.
В промышленности и технике более широкое распространение получили гетерогенные каталитические процессы. Гетерогенные каталитические процессы могут отличаться от гомогенных каталитических процессов более простыми методами отделения катализаторов от реакционной смеси, возможностью регулировать скорость процесса изменением состава и структуры активных центров и другими положительными свойствами. С учетом свойств твердых катализаторов создается структура реакционного устройства на промышленных установках.
Технологическая схема каталитического
производства ориентировочно
может
быть представлена следующей последовательностью операций и процессов.
1. Первичная переработка сырья с получением
основных реагентов
для
каталитического процесса;
2. Очистка реакционной смеси от примесей, засоряющих (пыль) или отравляющих (яды) катализатор;
3. Нагнетание газов или транспортировка жидких реагентов в реактор;
4. Подогрев реагентов до температуры катализа;
5. Катализ, обычно сопровождаемый отводом или подводом теплоты;
6. Переработка продуктов катализа в целевые
продукты производства.
Классификацию
катализаторов можно осуществлять при выделении основных признаков самих
катализаторов и каталитических процессов. Можно
выделить
следующие основные признаки для катализаторов и каталитических
процессов:
- агрегатное состояние катализаторов и реагентов (классификация по фазовому состоянию систем);
- способ разделения электронов между катализатором и реагентами (гомолитический и гетеролитический катализ);
- кислотно-основной катализ;
- химическая природа катализаторов;
- текстура твердых катализаторов;
- нанесенные и привитые катализаторы;
- биокатализаторы;
- межфазный катализ;
- нанокатализаторы.
Методы приготовления катализаторов
Исходным сырьем для производства
катализаторов обычно служат соли
каталитически активных металлов, золи, оксиды,
природные минералы. Выбор сырья определяется
составом катализатора, содержанием примесей, дефицитностью вещества и его
ценой. Оно должно удовлетворять определенным требованиям: постоянство
химического и фазового составов, отсутствие вредных примесей, необходимый размер частиц, нужная влажность,
возможно меньшая стоимость и т.д. Однородность
химического состава катализатора в значительной степени определяется
постоянством химического состава сырья, размером частиц в нем, влажностью, способом и продолжительностью
перемешивания исходных составляющих, а также
условиями транспортировки, загрузки и хранения.
Некоторые вещества в очень незначительных количествах сильно уменьшают активность и избирательность катализатора. Основное количество нежелательных примесей находится в сырье. Требования к чистоте исходных компонентов связаны со стоимостью конечного продукта. Другой возможный источник примесей – техническая вода, используемая для растворения, разбавления, промывки и т.д. При особо важных операциях в ряде производств используют очищенную или даже дистиллированную воду.
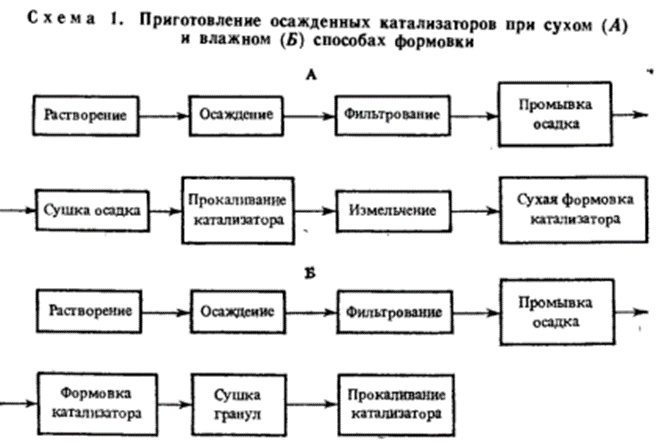
Способы формовки катализаторов и носителей: коагуляция в капле, экструзия, таблетирование, вмазывание пасты, гранулирование на тарельчатом грануляторе, размол материала, сушка в распылительной сушилке.
Формовку материала коагуляцией в капле и
сушкой в распылительной сушилке широко используют при изготовлении осажденных
катализаторов.
При экструзии влажный осадок выдавливают в виде шнура
из непрерывно
действующего шнекового или гидравлического пресса.
Форма и поперечный размер гранул определяются отверстиями в формующей
головке пресса. На выходе из головки шнур контактной массы режут вращающимся
ножом или натянутой струной, а образующиеся цилиндрики подхватываются ленточным
транпортером.
Таблетирование проводят
на таблеточных машинах под давлением 30
МПа. В зависимости от формы матрицы получают гранулы в виде цилиндров,
колец, седел, звездочек и т.д. В качестве связующих материалов используют
тальк, графит, жидкое стекло, некоторые органические кислоты.
Вмазывание пасты в отверстия перфорированной стальной пластины возможно для
гранулирования осадков различной природы и консистенции. Размер получаемых
гранул определяется толщиной пластины и диаметром отверстий. После подсушки
гранулы выбивают из пластины специальным штампом либо выдавливают сжатым воздухом.
Размол монолитных катализаторов осуществляют на дробилках и рабочую фракцию
отделяют на виброситах или в барабанных сепараторах. При этом
частицы имеют неправильную форму, наблюдается большое количество отходов и
пыли, но интервал получаемых размеров зерна может быть очень широк.
Гранулирование на тарельчатом грануляторе используют главным образом при изготовлении контактных масс механическим смешением компонентов.
Способы формовки влияют на удельную поверхность и пористую структуру контактных масс, в значительной степени определяют механическую прочность гранул, позволяя получать как очень прочные материалы (при коагуляции в капле, сушкой в распылительной сушилке), так и малопрочные (при таблетировании, экструзии и размоле).
Метод приготовления определяет степень дисперсности собственно каталитического компонента, форму, пористую структуру и активность контактной массы.
Заданный тип пористой структуры и удельную поверхность получают различными приемами в зависимости от природы изготавливаемого катализатора. В осажденных контактных массах это во многом зависит от условий осаждения, промывки и термообработки. Катализаторы, получаемые путем пропитки активными составляющими пористого носителя, сохраняют в основном его вторичную структуру. При сухом смешении компонентов пористость во многом определяется способом формовки, степенью измельчения исходной шихты, добавкой специальных веществ. Немаловажное значение на формирование структуры оказывают также температура и время термообработки катализатора.
Методом осаждения компонентов из растворов получают около 80% катализаторов и носителей. Этот метод позволяет в широких пределах варьировать пористую структуру и внутреннюю поверхность катализаторов и носителей.
Его недостаток в технологическом отношении – значительный расход реактивов, большое количество сточных вод. В зависимости от природы выпадающего осадка эти контактные массы условно можно разделить на солевые, кислотные и оксидные.
Примером оксидных осажденных катализаторов являются оксидножелезные контакты с различными промоторами, используемые при конверсии оксида углерода с водяным паром. В этом случае осадок представляет собой аморфный гидроксид железа в смеси с гидроксидами промоторов (хрома, висмута). При последующей термообработке полученные гидроксиды переходят в оксиды соответствующих металлов.
Различные силикагели,
алюмогели, алюмосиликаты, применяемые для
крекинга, гидратации, дегидратации, алкилирования и изомеризации
углеводородов, относятся к кислотным катализаторам. В процессе их получения при сливании
соответствующих растворов выпадает в осадок кремниевая или алюмокремниевая
кислота, гидроксид алюминия.
Образование солевых осажденных катализаторов сопровождается
выпадением соли, из-за которой в последующих технологических операциях может измениться
состав.
Растворение – процесс перехода твердой фазы в жидкую. В растворенном состоянии увеличивается подвижность и химическая активность молекул. В производстве осажденных катализаторов растворяют практически чистые твердые соединения (чаще всего соли в воде), перевод которых в раствор позволяет ускорить проведение последующих химических реакций.
Для приготовления растворов исходных веществ либо используют готовые кристаллические соли, либо растворяют соответствующие оксиды, гидроксиды, карбонаты в кислотах или щелочах.
Факторами, ускоряющими процесс растворения, являются перемешивание, температура, измельчение исходного сырья. Растворение проводят в реакторах с механическим или пневматическим перемешиванием. Возможно применение противоточных смесителей с механическим перемешиванием твердого материала навстречу потоку растворителя.
Осаждение – процесс образования твердой фазы в результате химической реакции при сливании растворов исходных компонентов. Переход растворенного вещества в осадок – совокупность двух процессов: образования зародышей твердой фазы и роста кристаллов или укрупнения гелеобразных частиц при одновременном их осаждении.
В зависимости от специфики получаемого катализатора к операции осаждения предъявляют определенные требования: полнота осаждения, селективность с целью освобождения осадка от нежелательных примесей, высокая степень однородности твердой фазы, характер осадка, состав исходного раствора, возможно меньшая стоимость осадителя.
Характер выделяющегося осадка (дисперсность, пористость, форма частиц) определяется температурой осаждения, рН среды, исходным составом раствора, его концентрацией, интенсивностью перемешивания, порядком слива растворов, условиями введения осадителя.
Периодическое осаждение, даже при получении однокомпонентных катализаторов и интенсивном перемешивании, дает неоднородный по составу продукт. Непрерывное осаждение позволяет получить более однородный катализатор, поскольку в этом случае все время сохраняются постоянными концентрация реагентов и рН раствора. При получении многокомпонентных и многофазных контактных масс достичь микрооднородности еще сложнее.
Вследствие различной растворимости осажденных соединений состав твердой фазы в начале и конце осаждения может оказаться неодинаковым. Это бывает при соосаждении смесей гидроксидов металлов из растворов солей.
Фильтрование.
В зависимости от свойств осадка и определяемых ими
свойств суспензии, а также специфики последующих операций
переработки
осадка используют фильтры разнообразных конструкций: барабанные,
дисковые вакуум-фильтры, фильтр-прессы и др. Отделение осадков от
жидкой фазы возможно также отстаиванием и центрифугированием. Наиболее
прост в аппаратурном отношении метод отстаивания. При неподвижном стоянии или
ламинарном течении системы под влиянием силы тяжести происходит
самопроизвольное оседание частиц осадка, поскольку плотность их больше
плотности жидкой фазы. Отстаивание суспензии проводят в аппаратах
периодического или непрерывного действия. При центрифугировании движущей силой
разделения твердой и жидкой фаз является центробежная сила, достигающая больших значений, под
действием которой осадок остается в роторе центрифуги, а жидкость удаляется.
Малое использование
этого метода обусловлено высокой дисперсностью и легкой сжимаемостью осадков,
высокой стоимостью и сложностью эксплуатации центрифуг.
