Лекция 2
| Site: | Satbayev University - Институт дистанционного обучения |
| Course: | Технология переработки тяжелой нефти / Айткалиева Гульзат Сляшевна |
| Book: | Лекция 2 |
| Printed by: | Гость |
| Date: | Monday, 2 February 2026, 10:54 PM |
1. Лекция 2. Характеристика основных серосодержащих соединений в нефти и нефтепродуктов. Методики выделения и использования серосодержащих веществ в промышленности.
Многие исследователи установили, что содержание сернистых соединений во фракциях нефтей непрерывно нарастает с увеличением температуры выкипания фракций.
В дистиллятах нефтей может содержаться до 70% сернистых соединений. Остальная часть сернистых соединений заключена в смолистоасфальтовой части нефти. Разумеется, такое распределение выдерживается не всегда, и некоторых нефтях большая часть сернистых соединений концентрируется в тяжелой смолистоасфальтовой части нефти.
Состав сернистых соединений не менее сложен, чем углеводородный состав нефти и нефтяных дистиллятов, в растворах которых они находятся.
В зависимости от группового состава сероорганические соединения можно условно разделить на три типа:
1 тип – меркаптановые, в которых в соизмеримы с сульфидами, дисульфидами и тиофенами количестве присутствуют меркаптаны; в таких нефтях возможно присутствие также сероводорода, дисульфидов и элементарной серы;
2 тип – характерен сульфидными соединениями, в которых преобладают сульфиды, в соизмеримом с ними или меньшем количестве имеются тиофены, а меркаптанов не более 5%;
3 тип – тиофеновые соединения, в которых содержатся преимущественно тиофены, сульфидов не более 10%, остальные сернистые соединения отсутствуют.
Наиболее распространены дисульфиды, в нефтяных фракциях их содержится приблизительно столько, сколько меркаптанов. Обычно дисульфиды присутствуют в фракциях, кипящих выше 110° С. С ростом температуры отгона их концентрация быстро падает и в дистиллятах, кипящих выше 300°С, становится почти неощутимой.
По мере возрастания температуры кипения дистиллятов количество полифункциональных сернистых соединений увеличивается. Больше всего этих соединений этого типа в нефтяных остатках.
Во фракциях, выкипающих до 180° С, значительную долю сернистых соединений составляют меркаптаны с тремя-четырьмя атомами углерода в молекуле, а во фракциях с температурами кипения 180 - 360° С сернистые соединения представлены, в основном, циклическими и сероароматическими соединениями, имеющими в молекуле 8 – 11 углеродных атомов.
Сера. Как известно, сера относится к числу широко распространенных в природе элементов. При обычных давлениях сера образует хрупкие кристаллы желтого цвета, плавящиеся при 112,80С; плотность ее 2,07 г/см3. Особенность этого элемента – сильно выраженная способность образовывать многочисленные аллотропные формы, различающиеся как числом атомов серы в ее молекуле (молекулярная характеристика аллотропа), так и взаимным расположением атомов и молекул серы в твердом состоянии (надмолекулярная характеристика аллотропа). Молекулы парообразной серы могут содержать от одного до двенадцати атомов серы – S; при содержании в молекуле более двух атомов серы последние легко образуют кольца. В жидком состоянии молекулы серы представляют циклические и короткие неразветвленные цепи; в твердом состоянии могут быть полимерные молекулы с числом атомов серы до 106. До настоящего времени описаны по крайней мере 12 твердых аллотропных форм серы, в том числе широко известных ромбической, моноклинной, а также полимерной. Вследствие большого числа модификаций физико - химические свойства серы, особенно в твердых состояниях, сильно зависят от условий ее предварительной обработки. Этим объясняются некоторые расхождения в параметрах, характеризующих ее отдельные свойства, которые приводятся в учебно-научной литературе.
При испарении растворителей из растворов серы с органическими растворителями, сера выделяется в виде прозрачных желтых кристаллов ромбической системы, имеющих форму октаэдров, у которых обычно часть углов или ребер как бы срезана. Эта модификация серы называется ромбической. Элементарная сера нерастворима в воде, но растворяется во многих органических растворителях.
Иной формы кристаллы получаются, если медленно охлаждать расплавленную серу и, когда она частично затвердеет, слить еще не успевшую застыть жидкость. При этих условиях стенки сосуда оказываются покрытыми внутри длинными темно-желтыми иголчатыми кристаллами моноклинной системы. Эта модификация серы называется моноклинной. Она имеет плотность 1,96 г/см3, плавится при 119,30С и устойчива только при температуре выше 960С. При более низкой температуре кристаллы моноклинной серы светлеют, превращаясь в октаэдры ромбической серы.
Сера широко используется в народном хозяйстве. В резиновой промышленности ее применяют для превращения каучука в резину; свои ценные свойства каучук приобретает только после смешивания с серой и нагревания до определенной температуры. Такой процесс называется вулканизацией каучука. Каучук с очень большим содержанием серы называют эбонитом; это хороший электрический изолятор.
В виде серного цвета серу используют для уничтожения некоторых вредителей растений. Она применяется также для приготовления спичек, ультрамарина (синяя краска), сероуглерода и ряда других веществ. Кроме этого она служит сырьем для получения серной кислоты.
Среди химических свойств отметим, в основном, те взаимодействия, которые могут сопровождать ее в составе нефти, нефтяных фракциях и газах.
Сероводород (H2S) – простейшее серосодержащее химическое соединение. При обычных условиях сероводород – бесцветный газ с неприятным запахом гниющего белка. Он немного тяжелее воздуха, сжижается при -60,33оС и затвердевает при -85,6оС. Вследствие этого, он концентрируется в нижних слоях атмосферы в районе выделения и медленно мигрирует в верхние слои.
Отличительной особенностью его является высокая токсичность. Следует заметить, что высокие концентрации по запаху не ощущается, так как он быстро парализует нервные клетки слизистой оболочки носовой полости человека. Сероводород образуется в природе в результате разложения органических соединений животного и растительного происхождения под воздействием бактерий, а также при гниении пищевых отбросов. Он встречается в вулканических газах и в водах минеральных источников. В лабораторных условиях обычно его получают действием разбавленных минеральных кислот на сернистые соли металлов (сульфиды).
Меркаптаны или их еще называют тиолы – обычные компоненты сернистых нефтей и газов.
Алифатические меркаптаны получаются при взаимодействии сероводорода с олефинами или спиртами. Так, например метилмеркаптан получается взаимодействием метилового спирта с сероводородом в паровой фазе в присутствии Al2O3, промотированного K2WO4.
Меркаптаны – слабые кислоты с резким специфическим запахом. Используют их в качестве одорантов бытового газа.
Сероуглерод – бесцветная жидкость с чрезвычайно неприятным запахом, хорошо растворяется во многих органических веществах – в спиртах, эфирах, хлороформе. Ни сероуглерод, ни его производные не содержатся в нефтях, но в незначительных количествах встречаются в некоторых природных газах.
Особенно они образуются в больших количествах в процессе очистки газов и газов нефтепереработки от сероводорода по методу Клауса на высокотемпературной стадии.
Одним из важнейших производных сероуглерода является сероксид углерода СОS – при обычных условиях это бесцветный газ без запаха, растворяется в сероуглероде, спиртах и толуоле.
Циклические соединения серы разделяются на 1) моноциклические (5-6 членные гетероциклы) и 2) полициклические. К первой группе относятся семейства тиофана (С4Н8S) и тиофена (С4Н4S), ко второй группе семейства бензтиофана (С8Н8S) и бензтиофена (С8Н6S). Они представляют собой жидкости с характерным неприятным запахом, содержится в нефти, в продуктах переработки нефти.
Основные методы извлечения сераорганических соединений из нефтей и нефтяных фракций
Наиболее надежные и доступные способы выделения сераорганических
соединений – окисление различными окислителями, адсорбция на силикагеле и оксиде алюминия, сернокислотная и щелочная экстракции. В каждом данном способе возможно много вариантов, различающихся природой используемого окислителя, экстрагента, катализатора окисления, растворителя, объемом технологических выбросов и т. Д. Из всех перечисленных методов, по-видимому, более перспективны способы, основанные на экстракционном принципе, которые привлекают простотой технологического воплощения и хорошо отработаны в промышленности.
Поэтому не прекращаются работы по подбору различных растворителей для выделения и концентрирования сернистых соединений нефти. Общими недостатками различных растворителей являются низкая селективность и достаточно высокая растворяющая способность в отношении парафинонафтеновых углеводородов. В связи с этим в процессах селективной очистки нефтепродуктов подбираются различные добавки к растворителям (спирты, воды), регулирующие селективность.
В соответствии со свойствами экстрагентов эти методы можно подразделить на три группы: кислотная, щелочная экстракция и экстракция органическими растворителями.
Для извлечения нефтяных сернистых соединений большой интерес представляет сернокислотная экстракция. Сернистые соединения или непосредственно растворяются в серной кислоте, или образуют в ней растворимые соединения. Сероводород окисляется серной кислотой до серы с образованием сернистого ангидрида и воды. Меркаптаны с серной кислотой образуют дисульфиды, сернистый ангидрид и воду.
Тиофен и его гомологи образуют хорошо растворимую в серной кислоте тиофенсульфокислоту. Сульфиды, дисульфиды и тиофены не реагируют с серной кислотой, но растворяются в ней и поэтому частично извлекаются из нефтепродуктов при сернокислотной очистке.
Сернокислотная экстракция - один из наиболее распространенных способов выделения сульфидов из низших и средних фракций нефти, несмотря на то, что он приводит к получению лишь сернисто ароматических
концентратов вследствие сравнительно слабой основности сульфидов и их
способности к ассоциации с конденсированными полициклоароматическими
соединениями. Для повышения степени концентрирования и глубины извлечения сульфидов с одновременным частичным их фракционированием
предложено обрабатывать нефтяные дистилляты водными растворами серной
кислоты с постепенно нарастающей концентрацией Н2S04.
Многоступенчатое сульфирование сернистых соединений с увеличивающейся концентрацией серной кислоты позволяет повысить полноту их извлечения до 95-97%. Остальные сернистые соединения, не извлекаемые концентрированной серной кислотой, следует отнести к весьма стабильным соединениям, структуру которых необходимо в дальнейшем изучить. Серная кислота пока единственный экстрагент, позволяющий получать концентрат с высоким содержанием сульфидов и испытанный в промышленном масштабе.
Впервые получена крупная партия концентратов сераорганических соединений нефтяных дистиллятов в опытно-промышленном масштабе методом сернокислотной экстракции. Метод применяется к высоко сернистым прямогонным фракциям, выкипающим в пределах 150-400 °С. Установлено, что в определенной концентрации серная кислотах хорошо растворяла сульфиды и не извлекала другие сернистые соединения и углеводороды. Наилучшие результаты достигаются при двухступенчатой экстракции. На первой ступени использовали 86%, а на второй - 91% серную кислоту. Выделенные сульфиды имели чистоту 85-87%. Но эта методика мало приемлема в случае фракций тяжелых высокосмолистых нефтей из-за сильного осмоления на стадии сернокислотной экстракции.
Основным достоинством метода экстракции серной кислотой является
возможность выделения устойчивых к действию кислоты сераорганических соединений с высоким содержанием сульфидов, а также повторного использования в качестве экстрагента обработанной серной кислоты, которая обладает высокой избирательностью при разделении сульфидов и углеводородов, большой стабильностью, позволяющей многократно регенерировать кислоту, высокой плотностью, способствующей быстрому и четкому расслаиванию фаз, доступна и дешева. Однако широкое внедрение этого метода в промышленность затруднено вследствие сильной коррозии оборудования, борьба с которой требует больших дополнительных затрат. Наряду с этим образуются трудно-утилизируемые кислые стоки и большое количество загрязненной воды, из-за этого метод сернокислотной очистки заменяется более перспективными методами.
Метод щелочной экстракции. Растворы щелочи преимущественно используются для извлечения слабокислотных сернистых соединений, например меркаптанов и сероводорода. Эти вещества реагируют со щелочью,
образуют соли, растворимые в воде и легко удаляющиеся с ней. При щелочной очистке из-за гидролиза невозможно достигнуть полного удаления меркаптанов. Чем больше молекулярная масса меркаптанов, тем труднее они извлекаются из нефтепродуктов. При щелочной очистке из нефтяных фракций можно извлечь 97,1% этил меркаптанов и только 33% изоамилмеркаптанов.
Для лучшего извлечения меркаптанов к щелочному раствору добавляют метанол, этанол, пропионовую кислоту, ароматические спирты и др. В качестве катализаторов окисления используют хлорную медь или сульфопроизводные фталоцианина кобальта, железа, ванадия и др. Традиционные промышленные варианты этого процесса, как гомогенные, так и гетерогенные, требуют больших объемов водно-щелочного реагента, что создает дополнительные экологические проблемы. В связи с этим большой интерес представляют бифункциональные катализаторы, позволяющие исключить или свести к минимуму использование щелочного агента. Катализаторы этого типа представляют собой системы, содержащие фталоцианиновые комплексы металлов (Со, Fe, Mn, V и др.) на носителе (уголь, смолы, оксиды металлов), поверхность которого имеет центры, обеспечивающие ионизацию молекулы RSH. Такие катализаторы характеризуются высокой активностью, однако в процессе работы быстро дезактивируются. В данной работе использовали бифункциональные катализаторы, которые готовили адсорбцией фталоцианина кобальта на минеральный оксидный носитель из водно щелочного раствора с последующим отмыванием избытка щелочи дистиллированной водой и высушиванием на воздухе. Процесс протекает через образование промежуточного тройного комплекса катализатор-меркаптан-кислород. В ходе исследований была проведена серия опытов и точно установлено, что основной вклад в отравление катализатора вносит побочный продукт реакции -сульфокислота. Поэтому эффект отравления катализатора может быть уменьшен введением в систему соединений, нейтрализующих сульфокислоту, например аммиака.
Методы комплексообразования
Комплексообразование с солями металлов является распространенным
способом выделения сераорганических соединений из нефтей и нефтяных фракций. Методы, основанные на комплексообразовании, привлекают простотой реализации, возможностью создания новых промышленно приемлемых способов получения концентратов сераорганических компонентов нефти и предварительной селективной очистки нефтяного сырья от сернистых соединений.
Сернистые соединения образуют стабильные комплексы с галогенидами металлов (Ti, Со, Hg, Pd, AI и др.), галогенами и галогенпроизводными соединениями, азотнокислыми серебром и др. Донорно-акцепторная связь осуществляется, вероятнее всего, за счет передачи неподеленной пары электронов атома серы на свободную валентную орбиталь металла. Комплексы R'RS- Me (CI)n легко не растворяются, как правило, в углеводородах и разрушаются после отделения при нагревании, обработке горючей водой или другими горячими растворителями, растворами щелочей.
Дисульфиды при взаимодействии с ацетатом ртути образуют растворимые комплексы, которые при обработке раствором хлористого натрия переходят в нерастворимое состояние. С увеличением молекулярной массы дисульфидов склонность к формированию комплексов уменьшается пропорционально увеличению доли углеводородной части. Это же явление наблюдается и для других сернистых соединений.
Первые методы комплексообразования для выделения сернистых соединений были связаны с использованием солей ртути, платины, палладия, серебра, цинка, алюминия и имели ограниченную применимость, поскольку использовались водные или водно-спиртовые растворы, а органические растворители не использовались из-за превалирующего влияния гидрофобной углеводородной части.
Методы окисления. Для извлечения сераорганических соединений из нефтей и нефтяных дистиллятов применяют окислительные методы, основанные на модификации функциональных групп. Окислителями являются пероксид водорода, азотная кислота, органические гидропероксиды, кислород воздуха в присутствии переходных металлов, их оксидов и сульфидов, гетерополикислоты и др. С наибольшей скоростью окисляются сульфиды, превращаясь в смесь сульфоксидов и сульфонов. С несколько меньшей скоростью меркаптаны окисляются до дисульфидов, полициклические тиофены - до сульфонов. Дальнейшее окисление может привести к образованию водорастворимых продуктов - алкансульфоновых кислот и, наконец, серной кислоты. Вместе с сернистыми соединениями окисляется часть ароматических углеводородов. Полученную сложную смесь разнообразных продуктов окисления можно от-делять от неокисленных углеводородов обработкой водой, а в некоторых случаях хроматографически. Большой интерес представляет окисление сульфидов до сульфоксидов и сульфонов. Окисление сульфидов до сульфоксидов проводят в мягких условиях (при комнатной температуре) 30% раствором пероксида водорода в гетерогенной среде в присутствии эмульгатора и каталитического количества концентрированной серной кислоты. Пероксид водорода берется с таким расчетом, чтобы окислить сульфиды только до первой стадии окисления - сульфоксидов. Степень превращения сульфидов 70-80%. Можно считать, что этот метод пригоден для промышленного применения.
Влияние минерально составляющих на качество нефтепродуктов и нефти, наличия в них металлов
Во всех нефтях наряду с углеводородами имеется значительное количество соединений, включающих такие гетероатомы, как сера, кислород и азот. Содержание этих элементов зависит от возраста и происхождения нефти.
Сера может составлять от 0,02 до 7,0 %, что отвечает содержанию сернистых соединений приблизительно 0,2—70%. К малосернистым относят нефти Марковского месторождения (Иркутская область) — 0,004 % серы, сураханскую нефть — 0,13%, балаханскую — 0,19% ; к сернистым и многосернистым — арлан-скую — 3,04%, уч-кызылскую — 5—7%, нефт
Таким образом, строение алифатических кислот тесно связано со строением алифатических углеводородов тех же фракций и изменяется по аналогичным законам.
Алициклические кислоты особенно характерны для нефтей нафтенового основания. Их содержание в различных нефтях колеблется от 0,03 до 3,0 %.
Нафтеновые кислоты были обнаружены Эйхлером еще в 1874 г. при очистке керосиновых фракций щелочью. Долгое время термин «нафтеновые кислоты» отождествлялся с термином «нефтяные кислоты». До некоторой степени это объясняется тем, что раньше нефти добывали с небольшой глубины и это были в основном молодые нефти нафтенового основания, в которых на долю нафтеновых кислот приходилось 90—95 % от суммы всех содержащихся в нефти кислот.
В нефтях обнаружены нафтеновые кислоты, содержащие от 1 до 5 полиметиленовых колец в молекуле. Моно- и бициклонафтеновые кислоты построены в основном из циклопентановых и циклогексановых колец. Карбоксильная группа может находиться непосредственно у углеродного атома кольца или отделена от него одной или несколькими' метиленовыми группами. Полиметиленовое кольцо может иметь от одного до трех метальных заместителей, причем довольно часто при одном углеродном атоме кольца может быть два метильных заместителя (гем-замещение).
Считается, что в полициклонафтеновых кислотах все циклы сконденсированы в единую систему, причем циклы в основном шестичленные. Сведения о кислотах с неконденсированными полиметиленовыми кольцами отсутствуют. Трициклические нафтеновые кислоты по содержанию в нефти уступают моно- и бициклическим и составляют на нефть не менее 0,05 %. Тетрациклических нафтеновых кислот меньше — 0,033 %, для них характерна стероидная структура. В последнее время идентифицированы несколько кислот типа:
и месторождения Гела — 7,3%, Этцель — 9,6% и нефтяные проявления Роузл Пойнт— 14 % серы.Кислорода в нефти содержится от 0,05 до 3,6 %. Это соответствует примерно 0,5—40 % кислородсодержащих соединений. Наиболее богаты кислородом бакинские: сураханекая — 0,52%, балаханская — 0,42 %, а также нефти Осиновского месторождения (Пермская область)—0,97% и Долииского месторождения (Украина) —0,72 %.
Содержание азота в нефтях не превышает 1,7 %. В нефтях СНГ азот встречается в пределах от 0,01 (марковская нефть) до 0,4% (ярегская нефть). Исключение составляет уч-кызыл-ская нефть — 0,82 %.
Распределение гетероатомов по фракциям нефти неравномерно. Обычно большая их часть сосредоточена в тяжелых фракциях и особенно в смолисто-асфальтеновом остатке. В зависимости от вида нефти фракции, перегоняющиеся выше 400— 450 °С, могут полностью состоять из гетероатомных соединений. Содержание смолисто-асфальтеновых соединений выше в молодых нефтях, и поэтому они обычно содержат больше гетероатомных соединений.
Элементный и групповой состав, а также физико-химические свойства нефтей даже одного месторождения часто заметно различаются в зависимости от глубины и места залегания. Например, нефти ромашкинского месторождения, относящиеся к отложениям девонского периода, имеют плотность 0,8620 и содержат 1,61 % серы, тогда как нефти того же месторождения, но более молодых отложений карбона имеют плотность 0,8909 и содержат серы 3,5 % То же можно сказать о нефтях Бавлинского месторождения, девонские содержат 1,4% серы, а нефти карбона — 2,8%. Аналогичная картина наблюдается в нефтях месторождений Западной и Восточной Сибири. Содержание серы в усть-балыкской нефти в зависимости от горизонта добычи колеблется в пределах от 1,40 да 2,06%, а нефти Марковского месторождения Восточной Сибири — от 0,004 до 0,89 %.
К минеральным компонентам нефти относят содержащиеся в нефти соли, образованные металлами и кислотами, металлические комплексы, а также коллоидно-диспергированные минеральные вещества. Элементы, входящие в состав этих веществ, часто называют микроэлементами, содержание которых колеблется от 10-8 до 10-2 %¦
Кислородсодержащие соединения
Кислородсодержащие соединения в нефтях редко составляют больше 10 %. Эти компоненты нефти представлены кислотами, фенолами, кетонами, эфирами и лактонами, реже ангидридами и фурановыми соединениями. Их относят к различным классам соединений, тождественным по структуре углеродного скелета углеводородам данной фракции нефти.
Содержание кислорода в нефтяных фракциях возрастает с повышением их температуры кипения, причем, по данным А. Ф. Добрянского, до 90—95% кислорода приходится на смолы и асфальтены.
Количество кислородсодержащих соединений нефти тесно связано с ее геологическим возрастом и характером вмещающих пород. Так, по обобщенным данным, полученным при анализе различных нефтей, установлено, что среднее содержание кислорода (в %) возрастает от 0,23 в палеозойских отложениях до 0,40 в кайнозойских для терригенных (песчаных) пород коллекторов. Содержание кислорода в нефтях, связанных с карбонатными породами, также убывает с увеличением возраста нефти, но оно всегда выше, чем в терригенных породах (0,31 % в палеозойских отложениях).
Наиболее распространенными кислородсодержащими соединениями нефти являются кислоты и фенолы, которые обладают кислыми свойствами и могут быть выделены из нефти или ее фракций щелочью. Их суммарное количество обычно оценивают кислотным числом — количеством мг КОН, пошедшего на титрование 1 г нефтепродукта. Содержание веществ с кислыми свойствами, как и всех кислородсодержащих соединений, убывает с возрастом и глубиной нефтяных залежей.
Трудность аналитического разделения кислот и фенолов до настоящего времени не позволяет с уверенностью говорить об их соотношении в нефтях. Если раньше было принято считать, что кислоты превалируют над фенолами, то по последним данным это утверждение справедливо только для палеозойских (старых) нефтей. В них содержание кислот (в пересчете на кислые продукты) колеблется от 52 до 80 %, а фенолов, соответственно, от 20 до 48 %. В мезозойских (средних по возрасту) нефтях кислоты составляют не более 58%, чаще менее 48%, а в кайнозойских (молодых) нефтях их количество не превышает 30—32%.
Еще менее достоверны сведения о количестве нейтральных кислородных соединений, особенно тяжелой (остаточной) части нефти, так как надежных методов их выделения пока не найдено.
Нефтяные кислоты. Наиболее изученный класс кислородсодержащих соединений нефти — нефтяные кислоты. Термин «нефтяные кислоты» подразумевает все алифатические, алициклические (нафтеновые) ароматические, гибридные (смешанного строения углеводородного радикала) кислоты, входящие в нефть. В бензиновых фракциях встречаются только алифатические кислоты, так как простейшие алициклические и ароматические кислоты кипят выше 200 °С. Эти кислоты имеют преимущественно нормальное или слаборазветвленное строение (с одним метальным заместителем в боковой цепи). Алифатические кислоты обнаружены также и в высококипящих фракциях. В настоящее время из нефтей выделены все кислоты нормального строения до 25 атомов углерода в цепи. По мере повышения температуры кипения нефтяных фракций в них появляются алифатические кислоты разветвленной структуры, содержащие два и более метильных заместителя в основной цепи. Наиболее интересной группой полиметилзамещенных алифатических кислот являются кислоты изопреноидной структуры. В настоящее время выделены с доказательством их строения 2,6,10-триметилундекановая; 3,7,11-триметилдодекановая; 2,6,10, 14-тетраметилпентадекановая (пристановая) и 3,7,11,15-тетра-метилгексадекановая (фитановая) кислоты:
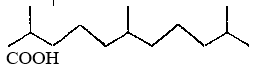
2,6,10-триметилундекановая кислота

3,7,11-триметилдодеканопая кислота
Таким образом, строение алифатических кислот тесно связано со строением алифатических углеводородов тех же фракций и изменяется по аналогичным законам.
Алициклические кислоты особенно характерны для нефтей нафтенового основания. Их содержание в различных нефтях колеблется от 0,03 до 3,0 %.
Нафтеновые кислоты были обнаружены Эйхлером еще в 1874 г. при очистке керосиновых фракций щелочью. Долгое время термин «нафтеновые кислоты» отождествлялся с термином «нефтяные кислоты». До некоторой степени это объясняется тем, что раньше нефти добывали с небольшой глубины и это были в основном молодые нефти нафтенового основания, в которых на долю нафтеновых кислот приходилось 90—95 % от суммы всех содержащихся в нефти кислот.
В нефтях обнаружены нафтеновые кислоты, содержащие от 1 до 5 полиметиленовых колец в молекуле. Моно- и бициклонафтеновые кислоты построены в основном из циклопентановых и циклогексановых колец. Карбоксильная группа может находиться непосредственно у углеродного атома кольца или отделена от него одной или несколькими' метиленовыми группами. Полиметиленовое кольцо может иметь от одного до трех метальных заместителей, причем довольно часто при одном углеродном атоме кольца может быть два метильных заместителя (гем-замещение).
Считается, что в полициклонафтеновых кислотах все циклы сконденсированы в единую систему, причем циклы в основном шестичленные. Сведения о кислотах с неконденсированными полиметиленовыми кольцами отсутствуют. Трициклические нафтеновые кислоты по содержанию в нефти уступают моно- и бициклическим и составляют на нефть не менее 0,05 %. Тетрациклических нафтеновых кислот меньше — 0,033 %, для них характерна стероидная структура. В последнее время идентифицированы несколько кислот типа:
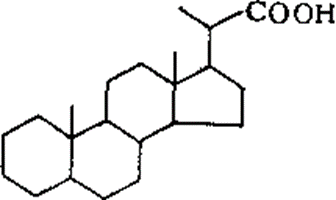
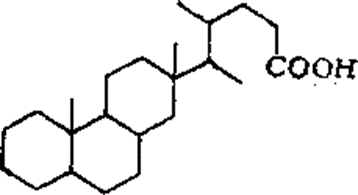
Ни одна из пентациклических кислот пока не выделена индивидуально. Они имеют строение, аналогичное строению кислот, выделенных из битуминозных пород.
Помимо алифатических и нафтеновых кислот нефти содержат разнообразные ароматические кислоты и кислоты смешанной нафтеноароматической структуры, которые имеют следующее строение молекул:
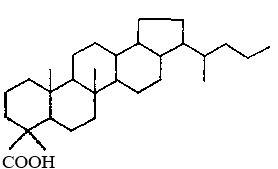
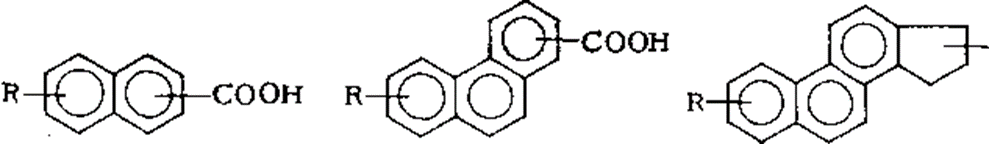
Кроме того, асфальто-смолистая часть нефти содержит асфальтогеновые кислоты — соединения, включающие помимо кислорода атомы серы и (или) азота. Строение их молекул пока не определено.
Нефтяные фенолы. Нефтяные фенолы, несмотря на значительное содержание их в нефти, изучены недостаточно. Наиболее известны низшие фенолы (С6—Cg). Например, в западносибирских нефтях наблюдается следующая закономерность в распределении фенолов, крезолов и ксиленолов: концентрация фенолов возрастает в ряду Св< С7«ССв< Сэ. Среди крезолов преобладает орто-изомер, а у ксиленолов — 2,4- и 2,5-диметилфенолы.
В высококипящих фракциях нефтей присутствуют фенолы,, содержащие в молекуле до 6 конденсированных колец, однако-их строение пока не расшифровано. Предполагают, что поли-циклические фенолы содержат насыщенные циклы с алкильными заместителями. С увеличением числа ароматических колец в молекуле фенолов уменьшается число алкильных заместителей.
Нейтральные соединения. Эти соединения изучены очень мало, и имеющиеся о них сведения не носят систематического характера. Одним из представительных классов этих, соединений являются кетоны. Из бензиновой фракции калифорнийской нефти выделено 6 индивидуальных кетонов: ацетон, метилэтил-, метилпропил-, метилизопропил-, метилбутил- и этил-изопропилкетоны. В некоторых нефтях кетоны составляют основную часть алифатических нейтральных кислородсодержащих соединений. В средних и высококипящих фракциях нефтей обнаружены циклические кетоны типа ацетилизопропилметилциклопентана и флуоренона:
К нейтральным кислородсодержащим соединениям нефти относят также сложные и простые эфиры. Большинство сложных эфиров содержатся в высококипящих фракциях или нефтяных остатках. Многие из них являются ароматическими соединениями, иногда представленными внутренними эфирами — лактонами. Имеются сведения, что в калифорнийской нефти найдены эфиры насыщенной структуры.
Простые эфиры, по мнению многих исследователей, носят циклический характер, типа фурановой структуры. Например, в калифорнийской нефти обнаружены соединения алкилдигидробензофураны (кумароны):
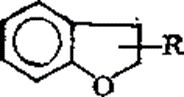
В западно-сибирской нефти найдены ди- и трибензофураны, а также их динафтенопроизводные.
Промышленное значение из всех кислородных соединений няефти имеют только нафтеновые кислоты, а более точно их соли — нафтенаты. Еще в начале XX века при очистке щелочью керосиновых и дизельных фракций нефти их стали получать как многотоннажный продукт. Большинство солей нафтеновых кислот не кристаллизуются, они имеют мазеобразную консистенцию и коллоидную структуру.
Благодаря хорошим поверхностно-активным свойствам нафтеновые (нефтяные) кислоты (техническое название «асидол») и их соли щелочных металлов («мылонафт») давно используют как моющие и чистящие средства, заменяя дефицитные животные и растительные жиры. Натриевые и калиевые соли нафтеновых кислот служат эмульгаторами при получении эмульсионных масел и деэмульгаторами при обезвоживании нефти. Нафтенаты кальция и алюминия являются загустителями при получении консистентных смазок, соли кальция и цинка — диспергирующими присадками к моторным маслам. Нафтенаты свинца, кобальта и марганца служат сиккативами (ускорителями полимеризации олифы) в лакокрасочной промышленности. Соли меди защищают древесину и текстиль от бактериального разложения. Соли алюминия в растворе, скипидара используют как лаки.